
引言
膜Shu前沿专栏致力于深度探索医学前沿,领略创新的魅力。在这里,我们将聚焦临床热点,解析未来诊疗趋势,为您呈现前沿文献资讯与深度解读。让我们一同倾听前沿之声,见证医学改变世界的力量。
2012年,针对复杂类型的腹主动脉瘤(AAA)的治疗选择有限。瘤颈长度在10-15mm以上,可以使用标准腹主动脉瘤腔内修复术(endovascular aneurysm repair,EVAR)支架完成。对于瘤颈长度在4mm以上的近肾腹主动脉瘤,可以使用的器械有成品化腹主开窗支架。然而,对于瘤颈长度不足4mm的病例,并没有专门为此设计的器械。
对于此类情况,治疗方式主要包括开放手术、去分支技术、平行支架技术、烟囱支架技术、八爪鱼技术、潜望镜技术、医生改良移植物技术(PMEG)以及激光原位开窗技术。
在2023年9月纽约血管腔内峰会(NYEVS)上,来自罗格斯大学的Beckerman教授介绍了腹主分支激光原位开窗术的见解及技术细节。
在欧洲,腹主分支激光原位开窗技术由法国外科医生Stephan Haulon推广。该技术在主体覆膜支架覆盖目标血管后,使用激光对覆膜材料进行打孔开窗,进而植入桥接支架。
在美国,Sukgu M. Han博士对腹主分支激光原位开窗相关技术研究的相当深入。其中心的一项单中心研究对比腹主分支激光原位开窗技术与其他技术(平行支架、PMEG、双管/反向髂支装置)在破裂SRAAAs(胸腹主动脉瘤)和TAAAs(肾上主动脉瘤)治疗中的效果。在此项研究中,激光原位开窗技术与改善生存率相关,特别是在低血压患者中,其住院死亡率降低了5倍。目前激光原位开窗技术已成为该中心的主要技术。
适用腹主分支激光原位开窗技术的类型主要包括:需要覆盖内脏分支血管的胸腹主动脉瘤或腹主动脉瘤的急诊患者、因紧急情况或其他因素而不适合PMEG(医生改良移植物技术)的患者、不适合开放手术的患者。
腹主分支激光原位开窗的禁忌症包括:1、目标血管周围的瘤体直径较大;2、动脉瘤极端扭曲;3、目标动脉开口向足侧严重转向,即使经上肢动脉入路也无法完成;4、主动脉严重锥形变细,导致目标血管附近支架的oversize过大;5、患者极度肥胖。
尽管激光原位开窗应用的病例往往情况较为紧急,但Beckerman教授仍强调需要适当的规划,主要考虑病变覆盖长度、瘤体直径、支架类型、靶血管直径、支架长度、成像角度、手术入路选择等。
在手术器械方面上,Beckerman教授倾向于选择涤纶主动脉覆膜支架,使用35系统长杆visi-Pros短支架做为内脏血管的预植入裸支架,使用35系统Viabahn VBX球扩覆膜支架作为桥接支架。其他器械包括12Fr DrySeal Flex亲水涂层导引鞘、7Fr/8.5Fr×55cm的Oscar可调弯鞘、Turbo-Elite 2.0mm激光导管、Navicross交换导管、18系统无聚合涂层的SvS-metal导丝、35系统长度260cmRosen工作导丝、4×20mm Sterling RX球囊、18系统5×20mm切割球囊及Mustang 8-10×20mm球囊作为喇叭口后扩张球囊。
Beckerman教授还分享了相关手术经验:术前将患者手臂固定于头顶支撑架有助于减少辐射并优化成像。在条件允许的情况下,尽可能使用图像融合技术。预先准备好所有导丝、导管和支架,并按照使用顺序进行放置。植入主动脉支架前记得校准激光光纤。此外,一个熟悉血管腔内治疗的团队同样十分重要。
首先建立通路,如果为非破裂或不稳定的瘤体,在主动脉覆膜支架植入前使用肝素将ACTs维持在约300s水平。在目标内脏血管预植入的支架一般选择较短、可扩张、高可视性的支架,并注意避免延伸至主动脉。在主动脉主体支架植入前记录能获取最佳影像视图的C臂角度。从主体支架植入时即启动缺血计时器记录缺血时间。植入主体支架后还要对靶病变区域进行球囊扩张。
理想情况下,需要根据重要性顺序开通内脏血管。Beckerman教授倾向于肠系膜上动脉、肾动脉、腹腔干动脉的顺序。配合可调弯鞘调整激光导管角度,使导管对准靶血管预植入支架的中心(建议在多角度视图下确保对准)。发射激光(60-60mJ/mm2),在激光导管穿透主体支架覆膜后立即推进导丝。确认导丝进入靶血管后移除激光导管,使用球囊序贯扩大开窗。交换导丝和球囊后在靶血管植入Viabahn VBX球扩覆膜桥接支架,最后用2cm球囊将VBX近端打成喇叭口装,来更好的固定分支支架。
Beckerman教授分享了一例腹主分支激光原位开窗病例报道。患者是一名79岁的男性,术前CTA显示该患者为Ⅳ型胸腹主动脉瘤,直径为6.2cm。
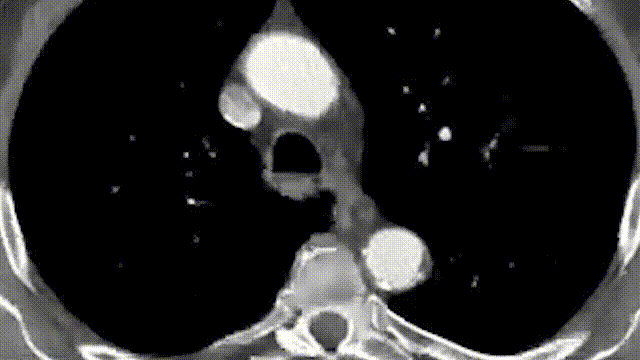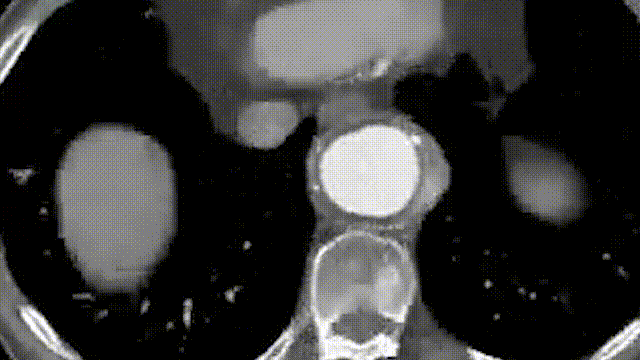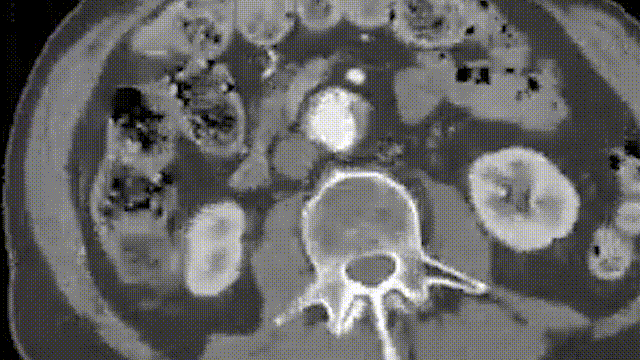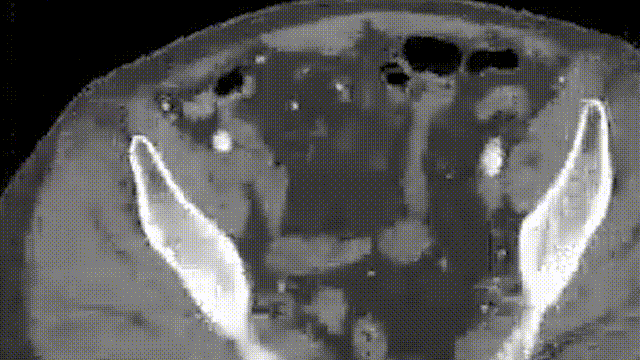
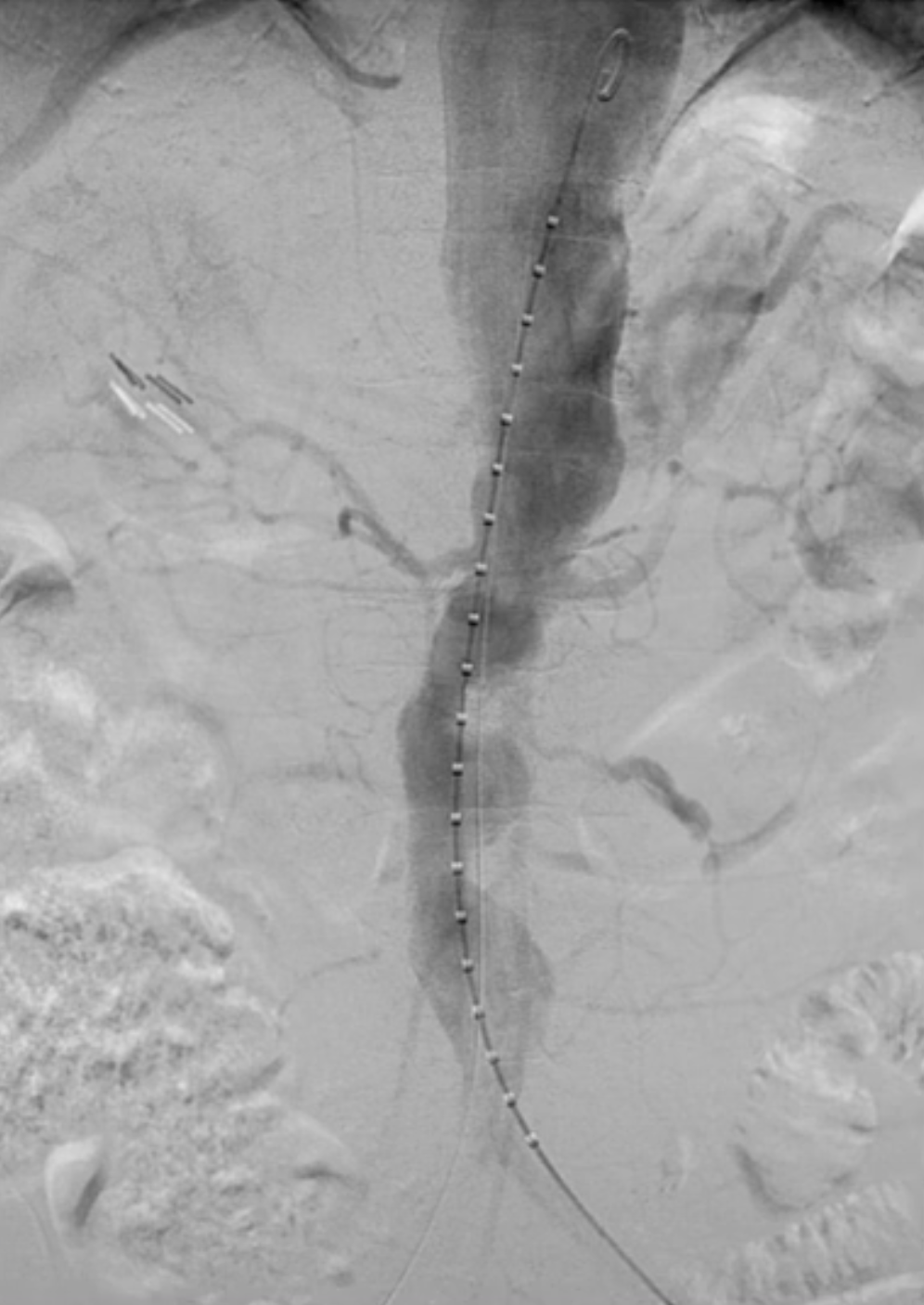
术前造影
使用12Fr DrySeal Flex亲水涂层导引鞘和7F可调弯鞘配合导丝超选入内脏动脉。
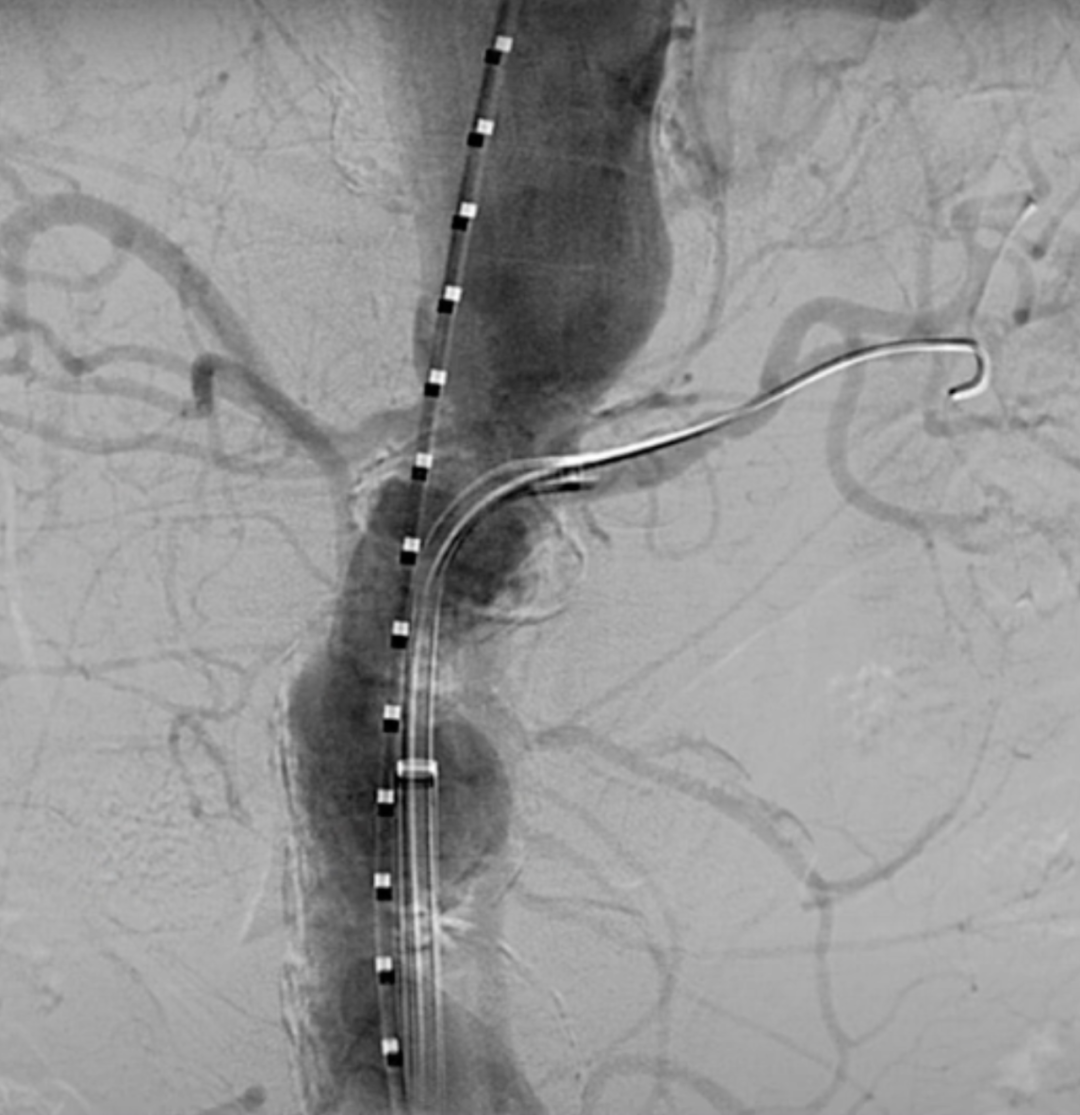
在左肾动脉预植入Visi pro裸支架。
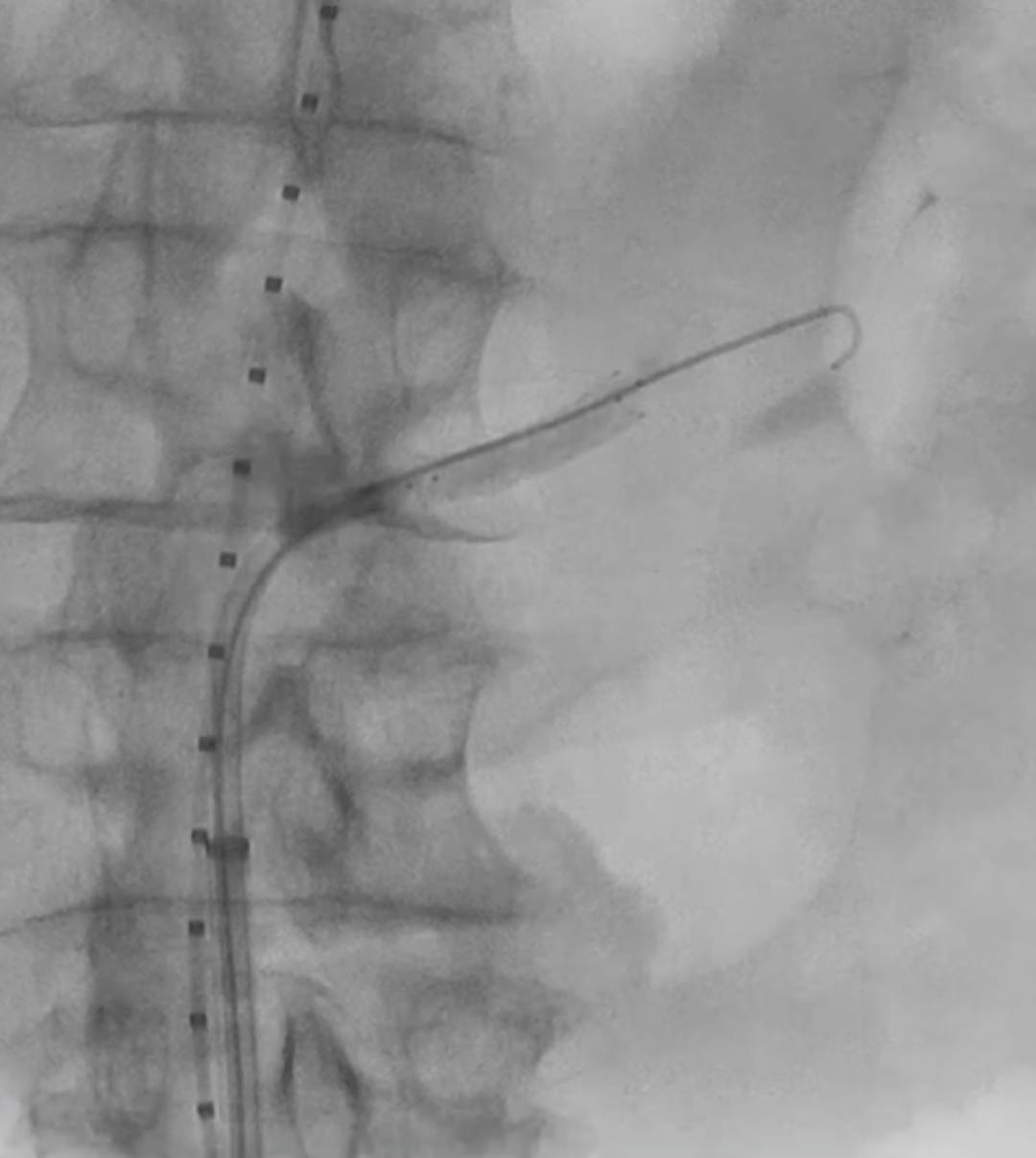
对其他目标内脏血管重复上述操作,在较弯曲的血管中选择较短的支架更为方便。在肠系膜上动脉进行必要的侧位造影。

在胃十二指肠动脉分叉前栓塞腹腔干动脉。
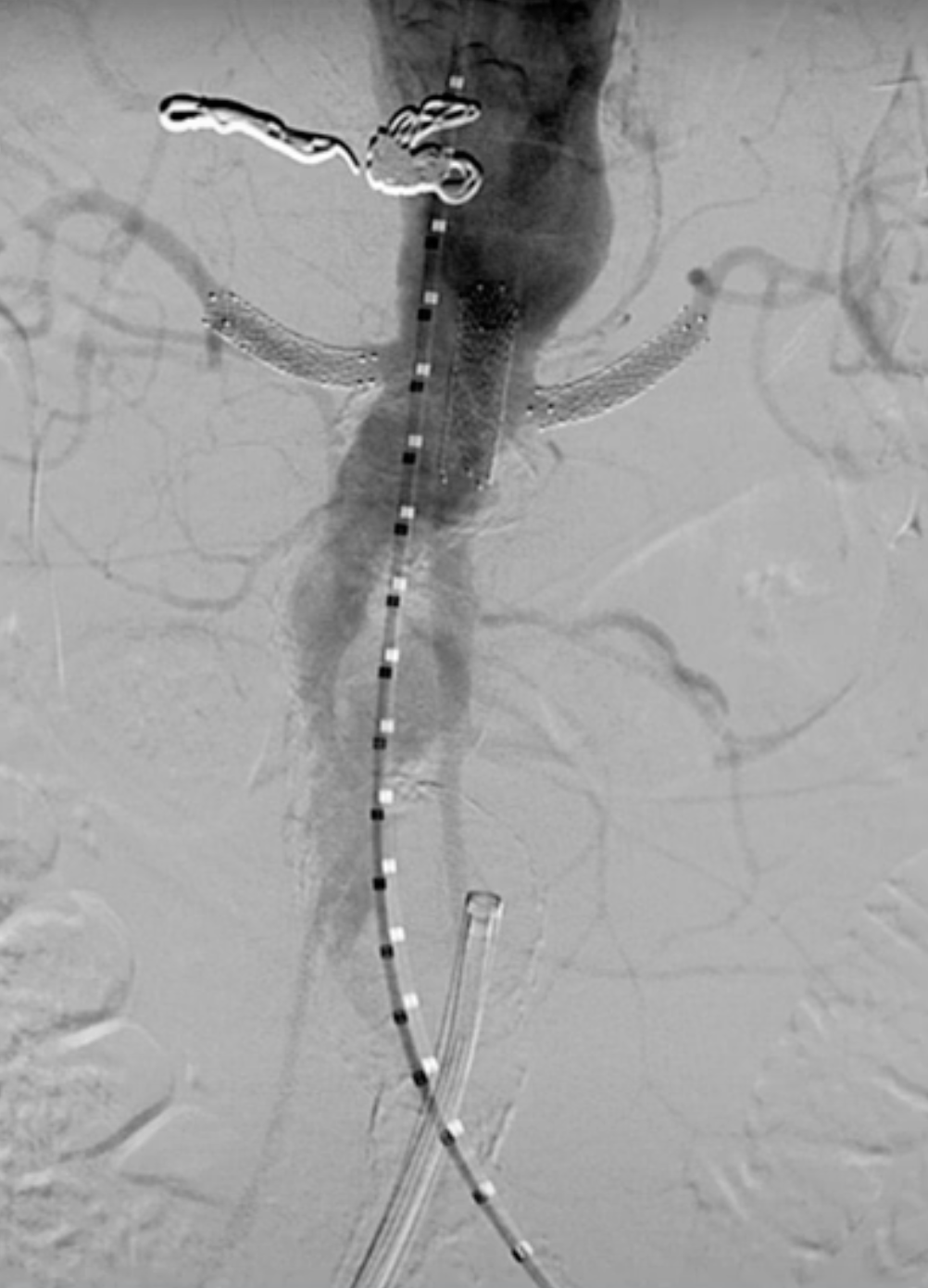
如果为非破裂或不稳定的动脉瘤,在植入主动脉覆膜支架前使用肝素将ACTs维持在约300s水平。

在植入主动脉支架后,首先开通SMA,配合可调弯导管调整激光导管角度,多角度视图下确保对准。发射激光(60-60mJ/mm2),激光穿透主体支架覆膜后立即推进导丝。

确认导丝进入靶血管后移除激光导管,依次使用4mm快交球囊、5mm切割球囊进行扩张开窗,交换入35系统导丝,在预植入的支架内引入VBX球扩覆膜支架,远端超过预植入支架远端,近端伸入主动脉3-5毫米,扩张球囊使VBX释放。
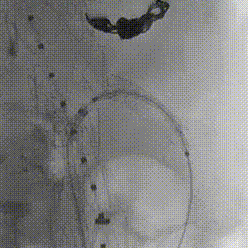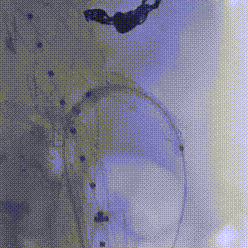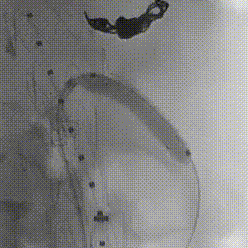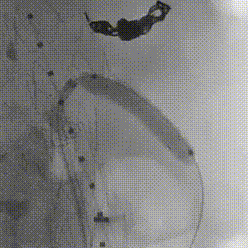
再次扩张VBX支架近端使其锚定于主动脉支架上。

造影确认开窗支架的通畅性。
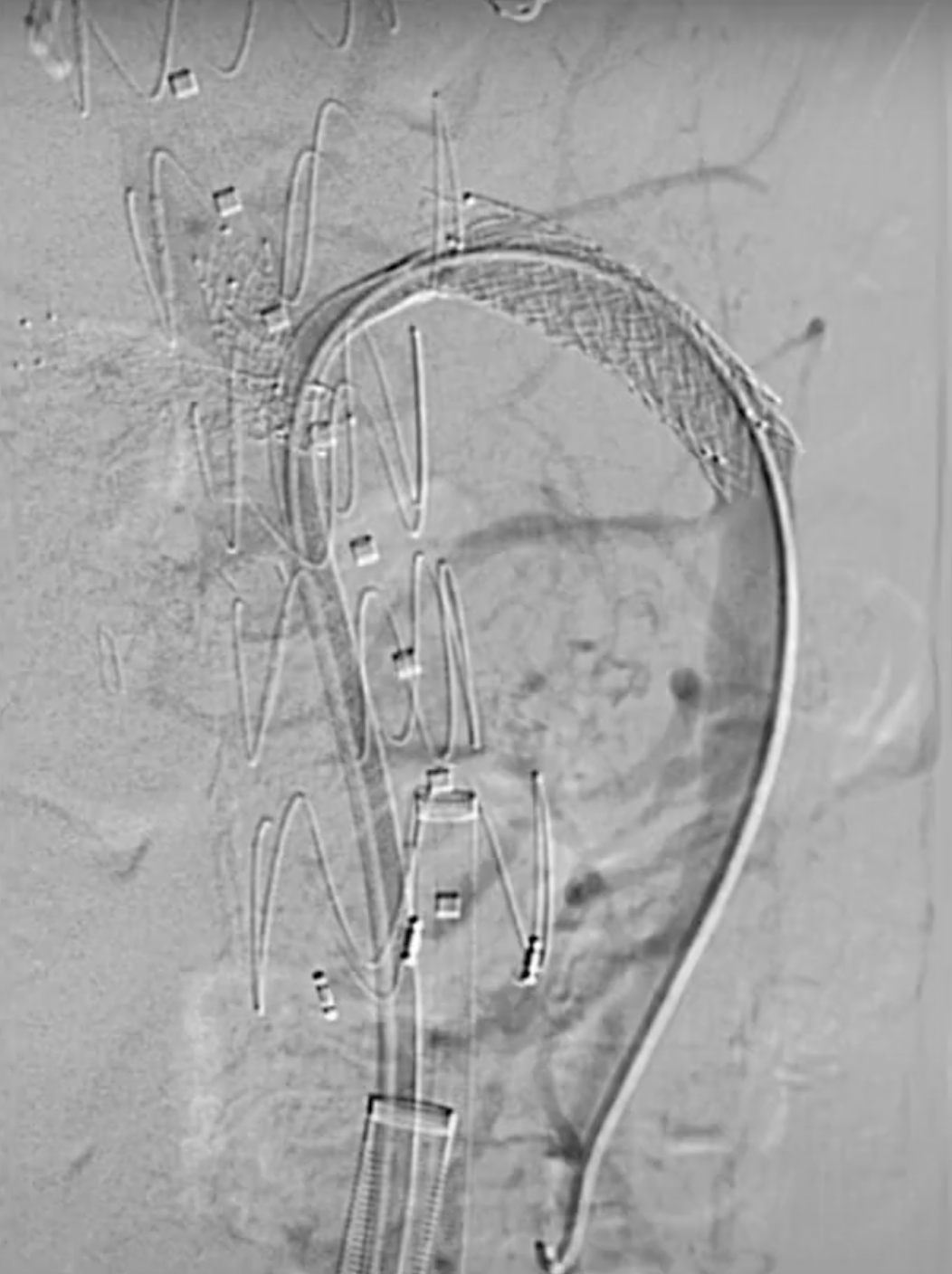
在其他目标动脉内重复以上操作。
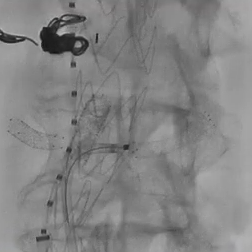
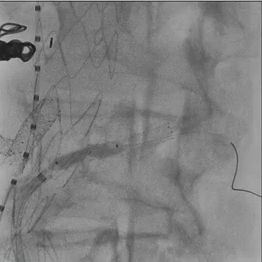
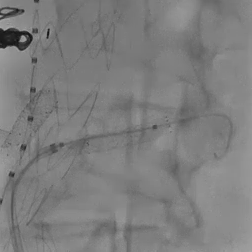

在激光开窗前多角度确认。

最后进行内脏动脉部分主动脉造影。注意在肾下有足够的空间(约5cm)以植入后续支架。使用普通EVAR支架完成后续的工作。

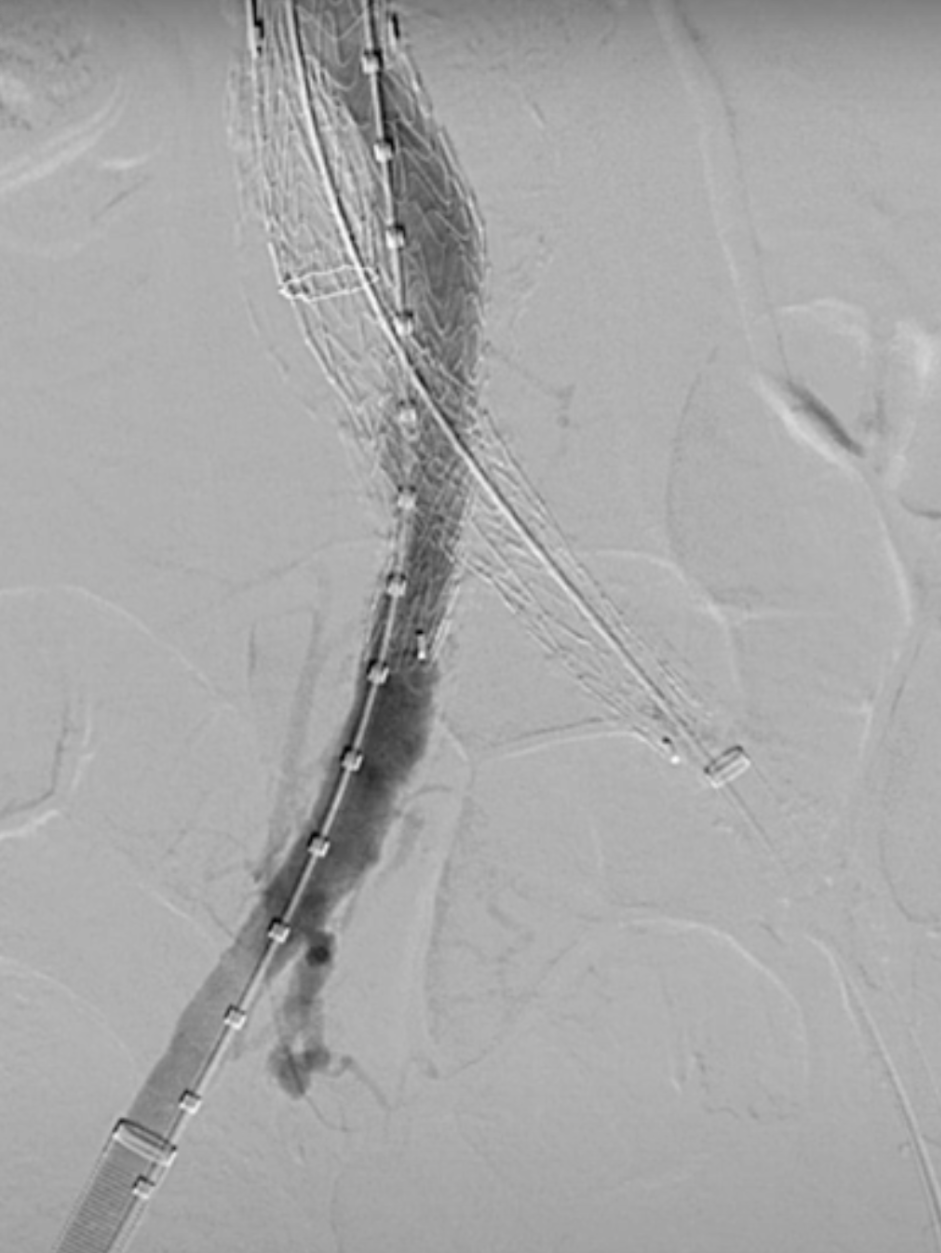
最后的正/侧位造影显示瘤腔隔绝满意,支架形态良好,主髂动脉及内脏分支动脉血流通畅。术中内脏动脉的总缺血时间<60min,肠系膜上动脉通畅在10-15min以内。
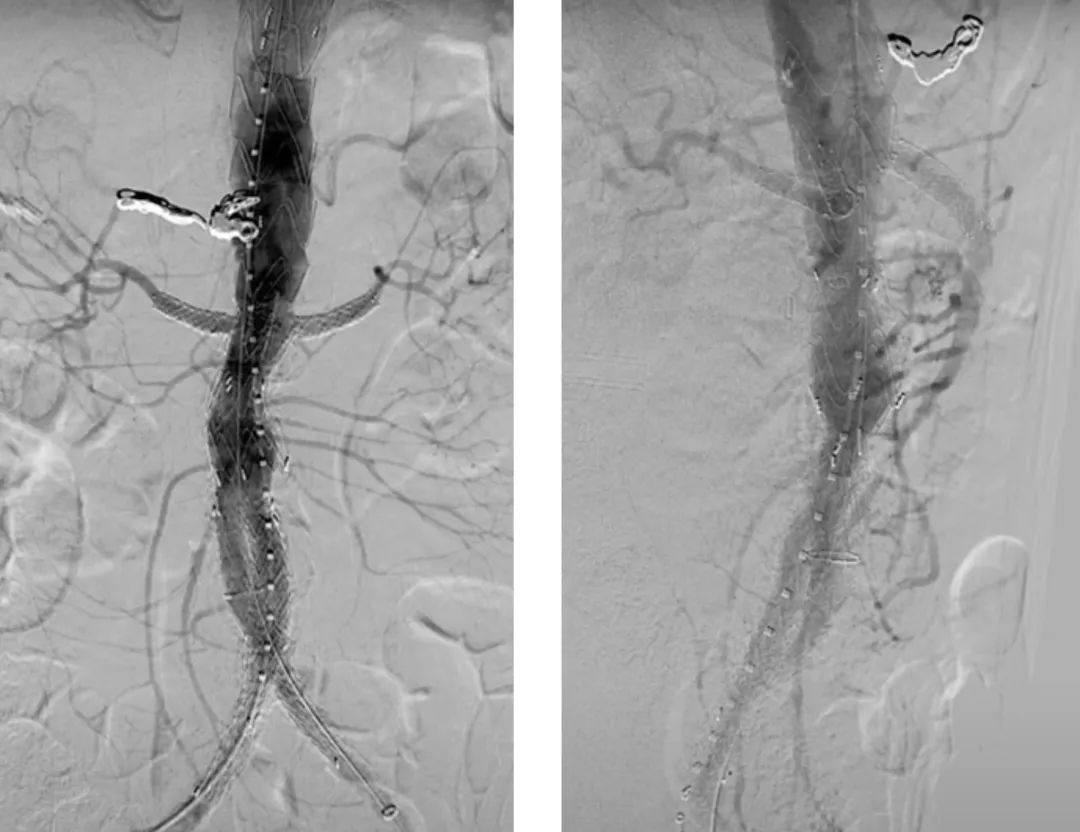
术后即刻造影
在Beckerman教授的病例分享中,提到了来自美国的Sukgu M. Han博士的一项单中心研究, 该研究于2022年10月发表在Journal of Vascular Surgery上,这项回顾性研究描述了一系列技术对破裂SRAAAs(胸腹主动脉瘤)和TAAAs(肾上主动脉瘤)进行修复的单一中心经验和相关结果。
该研究纳入了2014年7月至2021年3月期间接受破裂SRAAAs(胸腹主动脉瘤)和TAAAs(肾上主动脉瘤)血管内修复的42例患者,回顾性分析了临床表现、术中细节和术后结果,其中18例患者接受了激光原位开窗技术修复,并与接受非激光原位开窗技术修复的病例进行了对比。
表1 激光原位开窗技术与非激光原位开窗技术修复的人口统计学和术前特征
表2 激光原位开窗技术与非激光原位开窗技术修复术的术中细节
表3 激光原位开窗技术与非激光原位开窗技术修复的术后结果
结果显示,42例患者中,72%的激光原位开窗技术患者在手术前处于低血压状态,而非激光原位开窗技术组这一比例为46%。尽管激光原位开窗技术组每名患者平均纳入的分支血管数量更多(3.1 vs 2.2),但两组的总手术时间和透视时间相似。住院死亡率为19%,对于所有破裂情况,低血压患者的死亡率为25%。与非激光原位开窗技术组相比,激光原位开窗技术组的住院死亡率较低(11% vs 25%),在低血压患者中差异具有统计学意义(8% vs 45%,P = .048)。激光原位开窗技术和非激光原位开窗技术组之间不良事件发生率没有显著差异,术后肾功能不全(48%)是最常发生的并发症。在研究后期,激光原位开窗技术成为了该中心最常用的技术。
图3 应用于破裂胸腹主动脉瘤的腔内技术随时间的分布趋势(DB/rlBE:双筒隔绝/翻转式髂支技术;ISF:激光原位开窗技术;PG:平行支架技术;PMEG:医生改良移植物技术)
该研究得出以下结论,尽管紧急血管腔内修复破裂 SRAAAs/TAAAs 仍然是一个挑战,但有多种技术可用于急诊治疗。在这项研究中,激光原位开窗技术与改善患者生存率相关,特别是在低血压患者中,其住院死亡率降低了5倍,故激光原位开窗技术已成为该中心的主要技术。尽管有这些优点,术后尚存在并发症和再干预。未来需要更多的经验和长期随访来验证这些初步结果并评估其持久性。
END













